一种可降解NETs的注射用水凝胶,可治疗类风湿性关节炎
一种可降解NETs的注射用水凝胶,可治疗类风湿性关节炎


前 言
2023年来自吉林大学第一医院运动医学科的赵承武教授团队于《Drug Delivery, IF=6.5》杂志发表题为:一种可降解NETs的注射用水凝胶,可治疗类风湿性关节炎。作者开发了一种DNA功能化的水凝胶,通过不断降解NETs的新型药物靶点来降低类风湿性关节炎(RA)的炎症反应,进而治疗RA。本期小编将为大家分享这篇文章。
文章摘要
类风湿性关节炎(RA)是一种自身免疫性疾病,其特征是炎症细胞浸润损害软骨,破坏骨骼,损害关节功能。尽管目前治疗方法主要集中在抗炎活性上,但由于其复杂的病理机制,对RA严重受累侧的治疗效果仍不理想。最近发现RA发展机制涉及RA自身抗体与各种促炎细胞因子的相互作用,促进中性粒细胞胞外诱捕网(NETs)形成,从而增加炎症反应,表达炎症细胞因子和趋化因子。因此NETs结构降解可能抑制RA的正反馈炎症信号通路,减轻关节损伤。在这项工作中,脱氧核糖核酸酶I(Dnase)通过希夫碱反应与氧化透明质酸(OHA)连接,以延长DNase半衰期。该修饰不影响质粒脱氧核糖核酸水解的DNA酶活性和NETs结构分解。羧甲基壳聚糖与DNA功能化的DHA交联形成可注射、可降解、生物相容性好的水凝胶(DHY),进一步增强DHA粘附能力。重要的是胶原诱导关节炎模型表明,关节内注射DHY可显著降低炎症细胞因子表达,缓解RA症状,联合甲氨蝶呤可显著改善RA症状。本研究开发了一种DNA功能化水凝胶,通过不断降解NETs的新型药物靶点来降低RA的炎症反应,从而治疗RA。

结 果
DHY的制备与表征
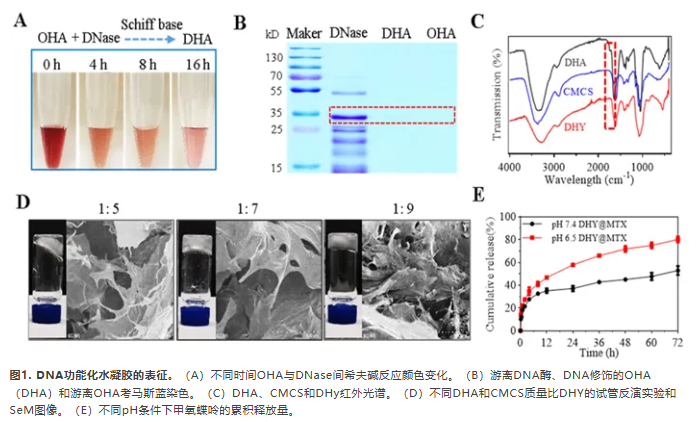
基于HA和壳聚糖等物理或共价交联聚合物,注射水凝胶已广泛用于蛋白质药物输送。然而水凝胶递送DNA酶靶向NETs结构消化治疗RA的疗效尚未得到评估。为解决这个问题,用NaIO4成功氧化HA(图S1),并通过酶的氨基和OHA的醛基间的希夫碱反应与DNase共价偶联。Purpald实验证实了DNase与OHA的结合,醛基还原后颜色发生变化。如图1(A)所示,随着反应时间的延长,颜色逐渐褪色。这表明 乙 基 与DNase发生了反应。此外,由于DHA的高分子量使其无法在凝胶电泳中移动,因此使用考马斯蓝染色来确认偶联反应(图2B和S2)。BCA法测定DNA酶在OHA中的质量比为15.5%。用DNase对OHA进行化学修饰,可以促进NETs结构的可持续降解。此外DHA上残留的乙醛基团可以与CMCS快速交联形成DHY(图S3)。通过FT-IR证实CMCS的氨基与DHA的醛基之间发生了席夫碱反应。在FT-IR上DHY醛基消失表明DHA和CMCS成功交联(图1C)。将不同质量比的DHA和CMCS混合,记录水凝胶稳定性和成胶时间,研究DHA和CMCS质量比对成胶性能的影响。试管倒置实验和SEM图像表明,当DHA和CMCS的比例分别为1:7时,DHA和CMCS可以在30 s内形成稳定的水凝胶,这被用于后续的研究(图1D)。膨胀实验在图S4中也显示相似结果。此外水凝胶已被广泛用于治疗药物的局部控制释放。因此将治疗RA的常用药物MTX包封在DHY中,促成疏水相互作用,其负载效率可达78.7%。由于RA关节腔是弱酸环境,研究不同pH条件下的释放行为。在pH为7.4和6.5条件下,前8小时有超过30%的MTX释放,这可能是由于DHY溶胀开始时释放突然,扩散迅速(图1E)。然而,pH为6.5显著加速MTX的释放,其中约80%和50%的MTX在pH为6.5和7.4时分别从DHY释放。这些结果表明,酸性环境可能促进DHY的降解和解离。
DHA介导体外NETs消化
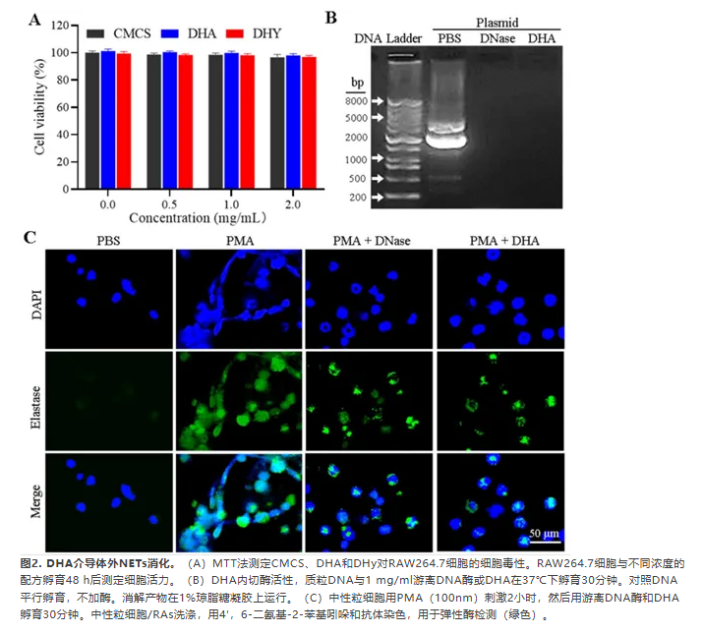
在小鼠巨噬细胞样细胞株RAW264.7对DHY中不同组分进行生物相容性评价。不同浓度CMCS、DHA和DHY与RAW264.7细胞孵育48小时(图2A)。最高浓度下两种聚合物均未表现出明显的细胞活力降低,表明DHY具有良好的生物相容性。重要的是,DHA可以消化质粒DNA,表明化学修饰不会影响DNA酶的活性(图2B)。因此用共聚焦法研究DHA是否能消化NETs结构。从小鼠骨髓中收集中性粒细胞用PMA处理,然后用游离DNA酶或DHA处理。中性粒细胞与PMA孵育2小时后,观察到典型的NETs结构,如图2(C)所示。然而经DHA或游离DNA酶处理后,NETs被降解并消失。这些表明,DNA修饰的聚合物不会改变酶活性,并可以消除NETs结构,这可能有利于NETs体内消化。此外研究DNase、DHA和DHY对PMA处理后中性粒细胞活化和细胞活力影响。如图S5A所示,PMA处理可以显著增加活性氧(ROS)释放,而DNase、DHA或DHY并没有改变中性粒细胞释放的ROS水平。因此DNase、DHA和DHY处理对PMA处理的中性粒细胞的细胞活力没有影响(图S5B)。
DHY体外抗炎活性
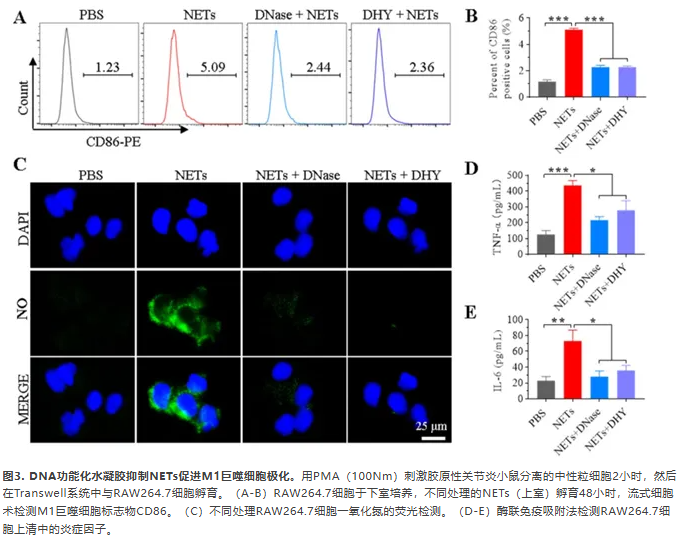
NETs通过激活巨噬细胞释放细胞因子来增加炎症反应。在RAW264.7细胞上检测DHA体外抗炎活性。如图3(A)、B和S6-S8所示,NETs处理可以促进巨噬细胞从M0向M1极化,表现为CD86和CD80表达增加。然而游离DNase或DHY处理可显著阻断NETs孵育引起的M1巨噬细胞极化。研究结果表明,DHY可能对减轻类风湿关节炎的炎症至关重要。一氧化氮(NO)作为炎症反应释放的重要指标之一,也能刺激NETs形成。因此我们检测了RAW264.7细胞释放的NO和炎症因子。图3(C)和S9显示,NETs处理后NO探针的荧光强度明显增加,说明NETs可能介导NO释放,促进炎症,而这两种作用均可通过游离DNase或DHY逆转。因此RAW264.7细胞培养上清中炎症因子TNF-α和IL-6显示,DHY处理可显著降低NETs培养巨噬细胞炎症因子的分泌(图3D和E)。
DHY体内释放行为
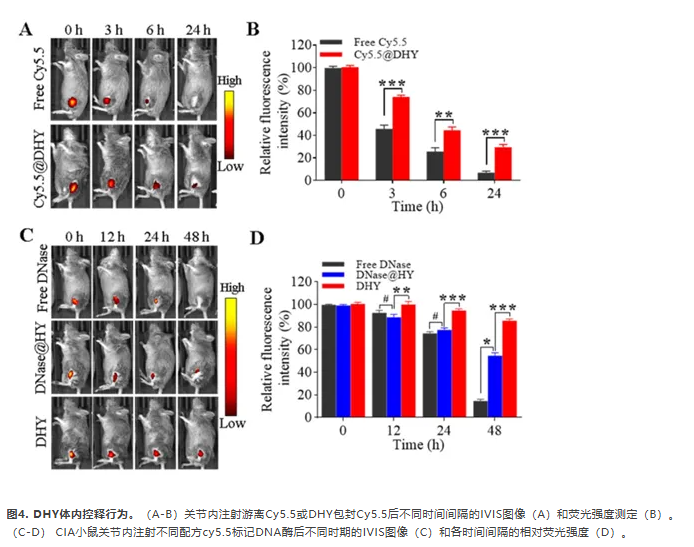
可注射水凝胶由于其控释特性,在类风湿性关节炎治疗中被广泛应用于给药。研究DHY体内控释行为,我们采用Cy5.5荧光染料作为模态染料。游离Cy5.5在关节内注射24 h后荧光迅速下降消失,如图4(A)、B所示。相比之下包被DHY的Cy5.5具有更持久的荧光,维持约30%荧光。体内释放速度快于体外MTX释放实验,这可能是由于Cy5.5的模态染料是水溶性的,容易从DHY扩散。此外将不同配方的cy5.5修饰的DNA酶注射到CIA小鼠关节腔中研究DNA酶在体内的行为。注射游离DNase、DNase@HY和DHY后,小鼠关节腔内可见强烈的荧光信号(图4C和D)。注射后48 h,游离DNA酶几乎没有荧光检测。当DNA酶包被水凝胶后,荧光强度降低40%以上。然而48 h后DHY荧光强度只有5%下降,说明DNase被固定在关节腔中并能在关节腔中长期保留。此外对DHY进行了长时间的荧光强度监测,结果显示在关节内注射15天后,可检测到约6%的荧光(Figure S10)。这些结果表明DHY具有良好的体内稳定性,可能具有阻止关节腔内NETs形成和减轻关节炎症的长效功能。
DHY的体内治疗效果
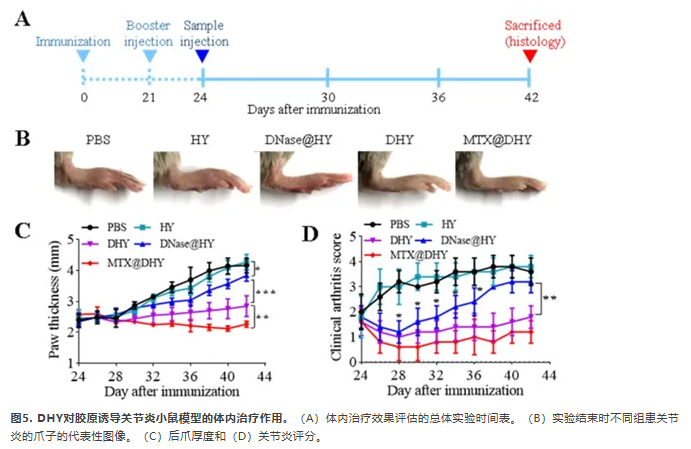
具有类风湿关节炎免疫学和病理特征的CIA小鼠被广泛用作类风湿关节炎治疗剂的研究模型。因此我们评估DHY和MTX对CIA小鼠的联合治疗效果(图5A)。对水肿、红斑和腿部僵硬CIA小鼠进行关节内注射PBS、HY、DNase@HY、DHY和MTX@DHY。PBS或HY治疗小鼠在所有实验期间均持续出现严重水肿和红斑。然而DNase@HY治疗小鼠的病理症状得到缓解,DHY和MTX@DHY治疗小鼠的病理症状几乎得到缓解(图5B)。从CIA建立的第24天开始,每2天记录一次爪周和关节炎评分(AI)。实验结束时PBS、HY和DNase@HY处理在爪周和AI方面没有显著差异,这可能是因为直接包被HY的DNase比共价偶联聚合物的DNase更容易释放和降解(图4C和D)。因此注射DHY小鼠在爪周和AI方面表现出明显的降低。DHY和MTX联合治疗的小鼠在治疗结束时达到接近正常小鼠的值。这些结果表明,联合应用MTX可显著增强靶向NETs消化以减轻RA的病理症状。
膝关节的组织学分析
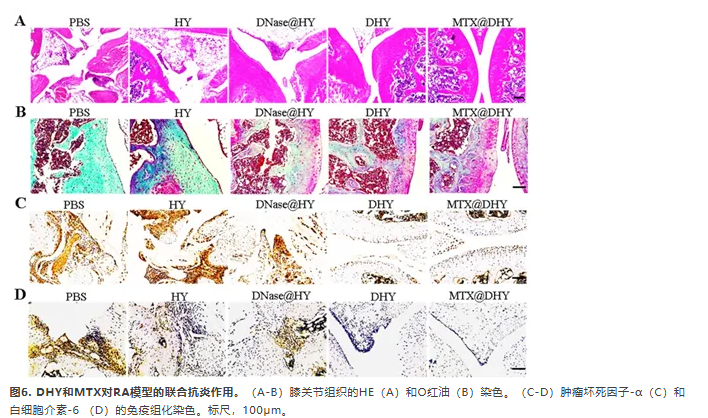
通过H&E和关节组织O红油染色进一步评价DHY治疗效果。如图6(A)所示,PBS或HY处理的RA小鼠出现了严重的软骨破坏和糜蚀,而DNase@HY处理的RA小鼠的病理状况较PBS或HY组小鼠弱。DHY组小鼠滑膜组织增生和软骨破坏水平明显降低。MTX联合DHY治疗效果最强,表现为关节面清晰。这些结果通过膝关节的O红油染色染色得到证实(图6B)。RA特点是炎症介质高表达。采用免疫组化染色检测经典炎症因子。DHY处理可显著降低TNF-α和IL-6表达,联合MTX可进一步降低TNF-α和IL-6表达(图6C和D)。这些结果表明DHY介导的NETs结构的体内消化可通过降低炎症因子的表达和阻断炎症信号通路反馈来缓解RA。
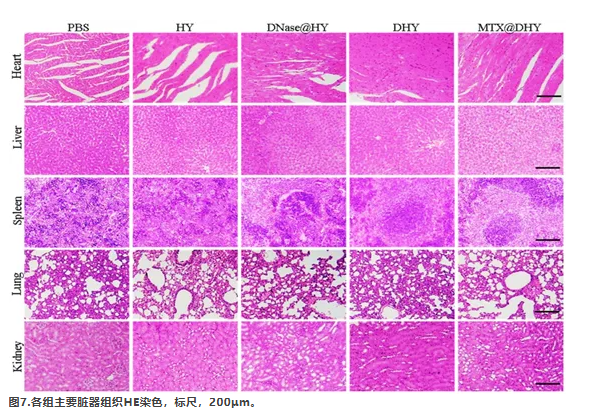
观察不同处理小鼠的体重变化,探讨丹参多糖的生物相容性。在实验期间,不同处理的小鼠体重没有显著差异(图S11)。此外通过对不同组小鼠的主要器官组织进行HE染色,评价DHY生物相容性。不同器官间未见病理改变,说明关节内注射DHY未引起全身毒性(图7)。
结 论
NETs是一种新机制,能促进炎症细胞因子和趋化因子表达,从而恶化关节微环境。本研究成功地设计了DHY用于NETs降解,并应用于缓解类风湿性关节炎(RA)。DNase与OHA共价偶联而不改变酶活性。此外DNA酶修饰的聚合物可以与CMCS快速交联,形成基于希夫碱反应的可注射水凝胶,这可以显著提高DNA酶在关节腔中的半衰期。DHY联合MTX对CIA小鼠模型有明显疗效,可降低炎症因子表达,且无明显副作用。因此靶向NETs降解的可注射水凝胶是一种很有前途的RA治疗策略。
参考文献:
PMID: 36724178 Doi: 10.1080/10717544.2023.2173332.